La terapia de rescate con fostemsavir continúa luciendo bien a las 96 semanas
Liz Highleyman 29 de julio de 2019
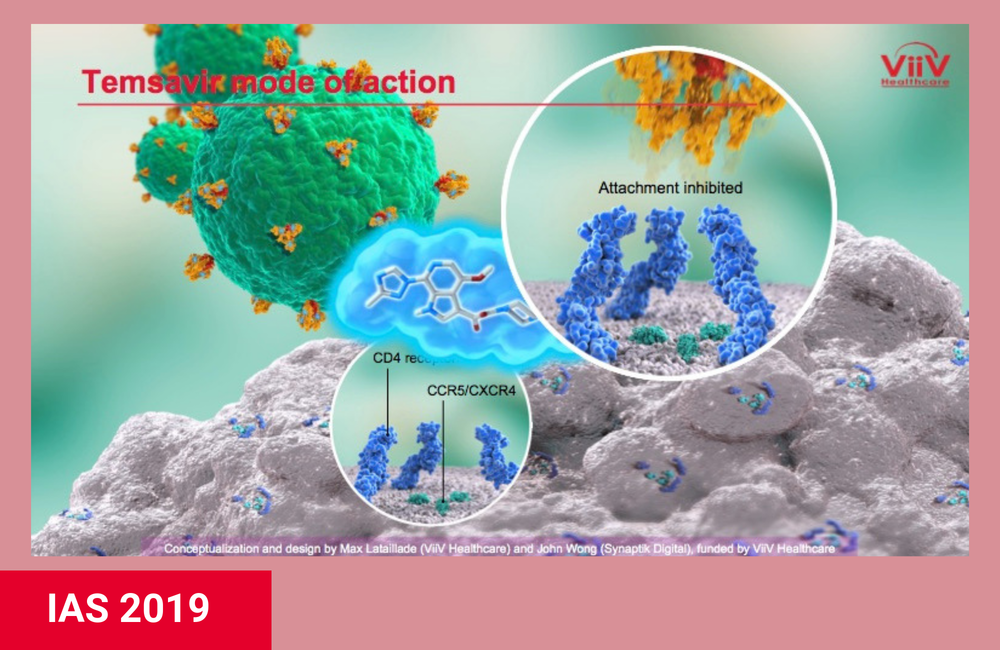
Crédito de la imagen: ViiV Healthcare
El nuevo inhibidor de la inserción del VIH, fostemsavir, continúa manteniendo la supresión viral en más de la mitad de las personas con experiencia extensa en el tratamiento previo y virus altamente resistentes, según un informe en la 10ª Conferencia de la Sociedad Internacional del Sida sobre la Ciencia del VIH (NIC 2019) en la última semana en México Ciudad. Los participantes del estudio, muchos de los cuales tenían supresión inmunológica avanzada en la línea de base, experimentaron ganancias sustanciales en las células CD4.
Fostemsavir es el primer antirretroviral oral que evita que el VIH se adhiera a las células huésped. Su forma activa, llamada temsavir, se une a la porción gp120 de la proteína de la envoltura del VIH que forma los picos en la superficie del virus. Esto evita que el virus se adhiera al receptor CD4 en las células T y otras células inmunitarias, que utiliza para ingresar a las células. (El medicamento inyectable enfuvirtide [ Fuzeon ] se une a la porción gp41 de la proteína de la envoltura del VIH).
El Dr. Max Lataillade, de ViiV Healthcare, presentó los últimos hallazgos del estudio BRIGHTE de fase 3, un ensayo en curso que evalúa fostemsavir en personas con un tratamiento intenso con VIH multirresistente que no pudieron desarrollar un régimen antirretroviral efectivo utilizando los medicamentos existentes.
La parte aleatoria del estudio incluyó a 272 participantes en un régimen que fallaba con virus no suprimidos (al menos 400 copias / ml). Fueron asignados a recibir 600 mg de fostemsavir dos veces al día o un placebo junto con su régimen fallido durante ocho días. Después de eso, todos recibieron fostemsavir de etiqueta abierta más un régimen de fondo optimizado que contenía los medicamentos más activos disponibles para ellos. Todos los participantes tenían que tener una o dos clases de medicamentos antirretrovirales restantes con al menos un agente aprobado completamente activo; El dolutegravir todavía estaba completamente activo durante aproximadamente el 65%.
En esta cohorte, alrededor de las tres cuartas partes eran hombres, la mayoría eran blancos y la edad media era de 48 años; El 60% tenía más de 50 años. La mayoría tenía una carga viral en el rango de 1000 a 100,000 copias / ml, pero el 29% tenía más de 100,000 copias / ml. La cuenta mediana de CD4 fue de 99 células / mm3, con un 72% con menos de 200 células / mm3 y un 26% con menos de 20 células / mm3. La mayoría tenía una historia de SIDA.
Además, 99 individuos a los que no les quedaban los fármacos aprobados totalmente activos se incluyeron en una cohorte de uso compasivo no aleatorizado. Este grupo podría usar otros agentes de investigación en su régimen optimizado, como el ibalizumab (que desde entonces ha sido aprobado en los EE. UU. Como Trogarzo y recientemente recibió una opinión positivade la Agencia Europea de Medicamentos). Esta cohorte fue demográficamente similar pero tenía una supresión inmunológica más avanzada, con un recuento de CD4 mediano de 40 células / mm3.
Como se informó en la Conferencia Europea del SIDA de 2017, el fostemsavir utilizado como monoterapia funcional redujo la carga viral más que el placebo durante los primeros ocho días. El ARN del VIH disminuyó en una mediana de 1.0 log10 en los participantes con una carga viral de referencia por encima de 1000 copias / ml, dijo Lataillade en la Ciudad de México, aunque previamente informó que la caída fue de 0.8 log10.
Lataillade presentó hallazgos de 48 semanas en el Congreso Internacional sobre Terapia de Drogas en la infección por VIH del año pasado en Glasgow. En ese momento, el 54% de los participantes asignados al azar a recibir fostemsavir y el 38% de los de la cohorte no aleatorizada lograron la supresión viral (<40 copias / ml).
En la semana 96, la proporción de pacientes aleatorizados con supresión viral aumentó al 60% en un análisis por intención de tratar. Las personas que cambiaron su régimen de fondo optimizado por razones de eficacia se contaron entre el 30% que experimentó una falla virológica. El otro 10% no tenía datos virológicos debido a la interrupción del tratamiento o la muerte. En un análisis observado o tratado, la tasa de supresión viral fue mayor, con un 79% con menos de 40 copias / ml y un 88% con menos de 400 copias / ml.
En la cohorte no aleatorizada, la tasa de supresión viral de 96 semanas se mantuvo estable en un 37% según el análisis por intención de tratar. Aquí, el 43% experimentó una falla virológica y el 19% no tenía datos virológicos. En el análisis observado, el 59% tenía un ARN del VIH inferior a 40 copias / ml y el 68% tenía menos de 400 copias / ml.
La reducción de la carga viral fue acompañada por una mejora en los conteos de CD4. La ganancia media a las 96 semanas en la cohorte aleatoria fue de 205 células / mm3, un aumento de 66 células / mm3 en la semana 48. La mejoría más grande (240 células / mm3) se observó en aquellos con menos de 20 células / mm3 al inicio. Entre las 71 personas que comenzaron con menos de 50 células / mm3 al inicio, el 56% tenía al menos 200 células / mm3 en la semana 96, el umbral para un diagnóstico de SIDA y un mayor riesgo de infecciones oportunistas. La proporción media de células CD4 a CD8 también aumentó. En la cohorte no aleatorizada, el aumento medio de CD4 fue de 119 células / mm3.
El tratamiento continuó siendo seguro y bien tolerado. Al observar ambas cohortes juntas, el 21% experimentó efectos secundarios de moderados a graves relacionados con el fármaco (grado 2-4), el 3% tuvo eventos adversos graves relacionados con el medicamento y el 7% suspendió el tratamiento debido a los eventos adversos. Los eventos adversos más comunes fueron náuseas, diarrea y dolor de cabeza. Además, hubo 38 (10%) eventos definitorios de SIDA y 29 (8%) muertes en esta población altamente inmunocomprometida; todas menos seis de las muertes fueron en personas con menos de 50 células / mm3.
«La respuesta virológica continuó mejorando con el tiempo a pesar del desgaste continuo en esta población difícil de tratar», concluyeron los investigadores del estudio. «Los resultados de BRIGHTE respaldan el desarrollo continuo de fostemsavir como una opción de tratamiento importante para las personas con mucha experiencia en el tratamiento que viven con VIH-1 resistente a múltiples fármacos».
Estos hallazgos muestran que fostemsavir «puede cambiar la vida de las personas que viven con el VIH y tener un recuento bajo de CD4», dijo Lataillade.
En respuesta a las preguntas de los defensores, reconoció que el programa de acceso temprano de fostemsavir (EAP) había sido limitado y que la solicitud de aprobación de la Administración de Drogas y Alimentos de los Estados Unidos (FDA) se había retrasado debido a problemas de fabricación. Sin embargo, dos nuevas instalaciones de fabricación se completaron recientemente y ViiV espera poder reabrir el EAP y espera presentar la aprobación de la FDA para fines de este año, según Lataillade.
Referencias
Lataillade JM et al. Semana 96: seguridad y eficacia del novedoso inhibidor de la inserción del VIH-1, fostemsavir, en participantes con gran experiencia en el tratamiento infectados con VIH-1 resistente a múltiples fármacos (estudio BRIGHTE) . 10a Conferencia de la Sociedad Internacional del SIDA sobre ciencia del VIH, Ciudad de México, resumen MOAB0102, 2019.
En: http://www.aidsmap.com/news/jul-2019/fostemsavir-salvage-therapy-continues-look-good-96-weeks

